27/03/2020
Multiparametrowe testy oceniające obecność w surowicy sIgE wobec molekuł alergenowych pozwalają na bardziej precyzyjną diagnostykę uczulenia u danego pacjenta, co przekłada się na możliwość spersonalizowania zaleceń terapeutycznych. Zatem, możemy powiedzieć, że diagnostyka molekularna alergii IgE zależnej jest kolejnym krokiem milowym w ziagnozowaniu alergii.
Badania epidemiologiczne ECAP w Polsce, pokazują znaczący wzrost występowania chorób alergicznych,w tym astmy i kataru alergicznego. W najbliższych kilku latach, przy obecnym tempie przyrostu tych chorób, liczba osób z alergią może zrównać się z liczbą osób zdrowych [1]. Pomimo, że lekarze diagnozujący choroby alergiczne mają do dyspozycji szeroki wachlarz narzędzi diagnostycznych, u wielu pacjentów nie udaje się z powodzeniem określić czynnika wywołującego reakcje alergiczne. Nowe korzyści przynoszą kompleksowe multiparametrowe testy III generacji do diagnostyki molekularnej alergii, umożliwiając oznaczanie immunoglobulin E swoistych nie tylko wobec ekstraktów, ale i molekuł alergenowych. W wielu przypadkach pomagają one precyzyjnie ustalić czynnik sprawczy alergii oraz prowadzą ku medycynie spersonalizowanej w alergologii.
Molekuły alergenowe
Możliwość diagnozowania alergii IgE-zależnej pojawiła się pod koniec lat 60. XX wieku w związku z odkryciem przeciwciał klasy E. Testy służące do oznaczania specyficznych immunoglobulin E (sIgE) in vitro do niedawna wykorzystywały w tym celu jedynie ekstrakty alergenowe. Pod pojęciem ekstraktu alergenowego rozumie się mieszaninę alergizujących oraz niealergizujących składników pochodzących ze źródła alergenowego, np. orzecha ziemnego.
Rozwój metod biochemicznych pozwolił na identyfikację w ekstraktach alergenowych poszczególnych składników, które są rozpoznawane przez sIgE [2]. Te składniki ekstraktów alergenowych nazywamy molekułami alergenowymi.
Odkrycie molekuł otworzyło nowy rozdział w diagnozowaniu alergii, pozwalając na lepsze zrozumienie podłoża objawów oraz możliwości występowania reakcji krzyżowych. Pierwsze narzędzia diagnostyczne umożliwiały detekcję w surowicy sIgE wobec pojedynczych molekuł. Najnowsze, wieloparametrowe testy do oznaczania sIgE w surowicy umożliwiają jednoczasowe oznaczanie nawet ponad 120 molekuł. Stanowią one krok ku terapii spersonalizowanej, dostosowanej do indywidualnego profilu uczulenia danego pacjenta [3].
Grupy białek
Bardzo dynamiczny postęp w odkrywaniu nowych molekuł alergenowych spowodował, że konieczne stało się uporządkowanie zdobytych informacji. W związku z tym podzielono molekuły na grupy na podstawie różnorodnych kryteriów, np. budowy czy funkcji (Tabela nr 1). Różna budowa molekuł alergenowych determinuje ich właściwości i stanowi podstawę do podzielenia molekuł na nadrodziny, rodziny i podrodziny.
Różne rodziny charakteryzuje różny stopień ryzyka wystąpienia anafilaksji czy reakcji krzyżowych (Rycina nr 1) [4].
Wśród rodzin molekuł pochodzenia roślinnego możemy wymienić między innymi białka zapasowe, nsLTP, Bet v-1 like, profiliny czy polkalcyny, podczas gdy wśród białek pochodzenia zwierzęcego mamy, np., tropomiozyny, lipokaliny, parwalbuminy, albuminy surowicze i inne.
Rodziny molekuł pochodzenia roślinnego
Molekuły z rodziny białek zapasowych
Molekuły z rodziny białek zapasowych, obecne w pokarmach pochodzenia roślinnego (np. w orzechach lub nasionach) mogą wywołać u pacjenta silne reakcje ogólnoustrojowe, włącznie ze wstrząsem anafilaktycznym po ich spożyciu. Białka te cechują się niskim stopniem występowania reakcji krzyżowych. W tej grupie znajdziemy takie podrodziny jak 2S albuminy, 7S globuliny czy 11S globuliny.
Nieswoiste białka transportujące lipidy – nsLTP
Kolejną szeroko rozpowszechnioną grupą występującą w pokarmach pochodzenia roślinnego są nieswoiste białka transportujące lipidy (nsLTP), których przedstawicielem jest np. molekuła brzoskwini zwyczajnej Pru p 3. Molekuły z tej grupy mogą być przyczyną lokalnych, ale i również silnych reakcji ogólnoustrojowych, wykazują one wysoki stopień reakcji krzyżowych.
Nadrodzina Bet v 1-like
Również powszechnie występującą w świecie roślin grupę stanowią białka należące do nadrodziny Bet v 1-like, której głównym reprezentantem jest molekuła brzozy Bet v 1. Do grupy tej należy aż 14 rodzin, wśród których jest rodzina białek Bet v 1. Jedną z 11 podrodzin grupy Bet v 1 jest grupa białek PR10, wśród których znajdują się takie homologi Bet v 1 jak: molekuła Ara h 8 orzecha laskowego, Gly m 4 soi, Api g 1 selera czy Cor a 1 leszczyny. Pacjenci uczuleni na białka tej grupy po kontakcie z alergenem najczęściej mają objawy miejscowe, a ryzyko ciężkiej anafilaksji jest niewielkie. Stopień reakcji krzyżowych pomiędzy homologami grupy Bet v 1-like jest wysoki [4].
Profiliny
Następną grupą są profiliny, które można znaleźć m. in. w lateksie oraz pyłkach traw i chwastów, rzadko dające objawy kliniczne u uczulonych pacjentów, a jeśli już takowe występują, mają lekki przebieg. Jednakże pomiędzy białkami tej grupy bardzo często dochodzi do reakcji krzyżowych.
Determinanty węglowodanowe CCD
Omawiając grupy pochodzenia roślinnego, należy wspomnieć również o grupie glikoprotein, jaką stanowią reagujące krzyżowo determinanty węglowodanowe CCD (Carbohydrate cross-reactive determinants). Obecne są one w alergenach takich jak: pyłki traw, żywność pochodzenia roślinnego (pomidor, seler, marchew, cukinia, jabłka orzeszki ziemne, laskowe, mango) w lateksie oraz jadach owadów. Mogą one w swoim składzie zawierać różne ilości węglowodanów, przyłączonych do białek, jako krótkie lub długie (do 15 jednostek), rozgałęzione lub nierozgałęzione łańcuchy.
Grupy tej nie można traktować jako jednego antygenu (ze względu na bardzo wiele różnych kombinacji strukturalnych), ale jako zbiór wielu antygenów szeroko rozpowszechnionych w przyrodzie, których rola w alergii nie jest do końca poznana [5, 6].
Pomimo że, wieloletnie obserwacje pacjentów, u których stwierdzono występowanie IgE anty-CCD wskazują na brak klinicznego znaczenia determinant węglowodanowych, to stanowią one jednak problem w zakresie diagnostyki serologicznej alergii, mogąc powodować fałszywie dodatnie wyniki oznaczeń sIgE wobec alergenów je zawierających [5, 7-10]. Od wielu lat trwają prace nad skuteczną metodą zablokowania anty-CCD, aby zminimalizować ich wpływ na wynik badania serologicznego [11].
Rodziny molekuł pochodzenia zwierzęcego
Lipokaliny
Jedną z najważniejszych grup molekuł pochodzenia zwierzęcego stanowią lipokaliny. Najwyższe ich stężenie znajduje się w ślinie, moczu, surowicy i naskórku zwierząt. Do tej grupy molekuł należą Can f 1 i Can f 2 psa, Fel d 4 kota, Equ c 1 konia oraz Bos d 2 o Bos d 5 krowy. Główną drogą narażenia na te alergeny są drogi oddechowe, za wyjątkiem alergenu Bos d 5 (β-laktoglobulina), która to molekuła jest alergenem głównym mleka krowiego [12]. Objawy u osób uczulonych na Bos d 5 mogą wystąpić po spożyciu surowego mleka krowiego.
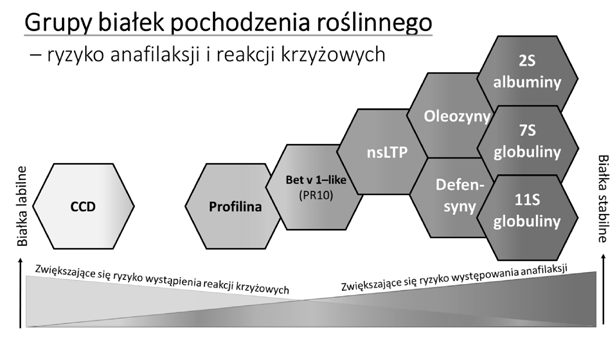
Ryc. 1 Rodziny molekuł alergenowych pochodzenia roślinnego z zaznaczeniem ryzyka poważnych reakcji alergicznychi reakcji krzyżowych
Tropomiozyny
Kolejną rodziną białek pochodzenia zwierzęcego są tropomiozyny, wśród których znajdują się m. in. molekuły roztoczy Der p 10 (Dermatophagoides pteronyssinus), Lit v 1 krewetki czy Ani s 3 nicieni (Anisakis simplex) pasożytujących w rybach morskich. Uczulenie na tropomiozyny wiąże się z wysokim ryzykiem wystąpienia wstrząsu anafilaktycznego, a ponieważ są grupą białek wysoce opornych na temperaturę, mogą powodować poważne reakcje nawet po spożyciu ich w postaci gotowanej [13].
Parwalbuminy
Inną grupą pochodzenia zwierzęcego są parwalbuminy, których najwyższe stężenie znajduje się w mięśniach ryb. Przedstawiciele tej grupy białek to Mer mr 1 morszczuka, Cyp c 1 karpia, Gad c 1 dorsza, Onc m 1 pstrąga, Sal s 1 łososia czy Thu a 1 tuńczyka. Jest to rodzina białek odpornych na działanie temperatury i enzymy trawienne. U osób uczulonych mogą wywoływać natychmiastowe systemowe reakcje po ich spożyciu, ale również mogą one powodować objawy poprzez opary wnikające do dróg oddechowych podczas smażenia ryb [12].
Białka zapasowe:
- 2S albuminy – Ara h 2 i Ara h 6 orzech ziemny, Jug r 1 orzech włoski,Ses i 1 sezam
- 7S globuliny – Ara h 1 orzech ziemny, Jug r 2 orzech włoski, Gly m 5 soja, Pis s 1 orzech piniowy
- 11S globuliny – Ara h 3 orzech ziemny, Gly m 6 soja, Cor a 9 orzech laskowy
Występują w orzechach i nasionach
Ryzyko ciężkich i ogólnoustrojowych reakcji alergicznych, np. reakcji anafilaktycznej
Alergizują nawet po obróbce termicznej, odporne na enzymy trawienne
Generalnie niski stopień reakcji krzyżowych pomiędzy gatunkam
NSLTP:
- Act d 10 kiwi zielone, Ara h 9 orzech ziemny, Cor a 8 orzech laskowy, Jug r 3 orzech włoski, Pru p 3 brzoskwinia, Pun g 1 granat, Sola l 6 pomidor, Par j 2 pokrzywa, Tri a 7k-LTP pszenica zwyczajna, Pis s 3 groch zwyczajny (zielony groszek) Zea m 14 kukurydz
Występują w owocach, warzywach, orzechach i pyłkach
Alergizują nawet po obróbce termicznej, odporne na enzymy trawienne
Mogą wywoływać silne reakcje ogólnoustrojowe, zespół OAS
Różny stopień reakcji krzyżowych pomiędzy gatunkami
BET V 1 – LIKE:
- Bet v 1 brzoza, Api g 1 seler, Ara h 8 orzech ziemny
- Cor a 1 orzech laskowy, Mal d 1 jabłko
Występują w owocach, warzywach, orzechach i pyłkach
Wrażliwe na obróbkę cieplną i enzymy trawienne, pokarmy zawierające te molekuły po podgrzaniu często są dobrze tolerowane
Wywołują zazwyczaj objawy miejscowe jak np.: zespół OAS
Różny stopień reakcji krzyżowych pomiędzy gatunkami
PROFILINY:
- Bet v 2 brzoza, Hev b 8 lateks, Mer a 1 szczyr roczny, Ole e 2 oliwka
Występują w pokarmach pochodzenia roślinnego, pyłkach traw, chwastów i drzew
Wrażliwe na obróbkę cieplną i enzymy trawienne, pokarmy zawierające te molekuły po podgrzaniu często są dobrze tolerowane
Rzadko powiązane z objawami klinicznymi (miejscowymi czy ciężkimi reakcjami)
Wysoki stopień reakcji krzyżowych pomiędzy gatunkami
CCD (RESZTY WĘGLOWODANOWE):
- Markery CCD – Hom s LF laktoferyna ludzka po glikolizacji w ryżu, Ana c 2 bromelaina ananasa, Arm r HRP peroksydaza chrzanowa, Sola t 1 patatyna ziemniaka
- CCD mogą zawierać: Cup a 1 cyprys, Jug r 2 orzech włoski, Lol p 1 życica
- Ole e 1 oliwka, Ara h 1 orzech ziemny, Api m 1 pszczoła
Występują w pyłkach, pokarmach pochodzenia roślinnego, jadach owadów
Mogą powodować wynik dodatni sIgE dla alergenów w których są obecne
Nie udowodniono jak dotąd związku z objawami klinicznymi
Bardzo wysoki stopień reakcji krzyżowych pomiędzy gatunkami
Albuminy surowicze
Albuminy surowicze to rodzina białek występująca w ślinie, moczu, naskórku, surowicy i mięsie zwierząt. Narażenie na te alergeny zazwyczaj występuje poprzez drogi oddechowe. Są to białka wrażliwe na działanie temperatury. Podobieństwo różnych molekuł należących do rodziny albumin surowiczych może powodować fałszywie dodatnie wyniki uzyskane przy pomocy punktowych testów skórnych. Wśród tej grupy znajdziemy molekuły Can f 3 psa, Fel d 2 kota, Equ c 3 konia, Gal d 5 jaja kurzego. Wśród tej grupy znajdziemy również molekułę Bos d 6 – która jest alergenem mniejszym mleka krowiego, ale alergenem większym wołowiny [12].
Diagnostyka molekularna – 2 różne podejścia
Międzynarodowe wytyczne oraz model “top-down” wskazują, że podstawowym narzędziem w diagnozowaniu alergii powinien być wywiad w oparciu o współistniejące objawy kliniczne [4, 14].
Drugim etapem jest przeprowadzenie testów opartych na ekstraktach alergenowych in vivo lub in vitro, a w trzecim kroku znajdziemy diagnostykę opartą o molekuły alergenowe. Jednak konsensus WAO-ARIA-GA2LEN 2013 – pokazuje, że doświadczony lekarz alergolog już w drugim etapie diagnostycznym może włączyć diagnostykę w oparciu o testy molekularne [15]. Zwłaszcza, że najnowsze wieloparametrowe testy III generacji do oznaczania sIgE pozwalają na oznaczanie jednoczasowe zarówno ekstraktów, jak i molekuł alergenowych, łącząc 2 i 3 krok diagnostyczny w jeden etap [16].
Ostatnio zaprezentowano model diagnostyczny „bottomup”, gdzie metody molekularne wykorzystywane są na samym początku diagnozowania alergii, i dopiero w dalszej kolejności wykonywane oznaczenia sIgE wobec ekstraktów in vivo lub in vitro, a uzyskane wyniki poddawane są interpretacji z analizą objawów towarzyszących [4, 17].
Zwolennicy podejścia “bottom-up” argumentują, że ekstrakty nie są standaryzowane, co może dawać fałszywy obraz uczulenia, a w rezultacie prowadzić do niewłaściwych decyzji terapeutycznych [4].
Komu przynosi korzyść diagnostyka molekularna
Istnieją określone grupy chorych, u których wykorzystanie narzędzi diagnostyki molekularnej alergii może w istotny sposób wpłynąć na decyzje terapeutyczne (Tabela nr 2.) [17]. Dzięki lepszej dokładności diagnostyki molekularnej w porównaniu do testów skórnych, liczba wizyt, czas potrzebny do postawienia prawidłowej diagnozy i dobrania odpowiedniej immunoterapii, mogą zostać zmniejszone, a to przełożyć się może na ogólną poprawę opieki nad pacjentem [19].
Wielu autorów w swoich badaniach wykazało, że u pacjentów z objawami alergii częściej występuje uczulenie wobec kilku alergenów niż wobec tylko jednego alergenu [20, 21]. Objawy alergii manifestujące się po kontakcie z wieloma alergenami mogą być spowodowane uczuleniem na nie lub występowaniem reakcji krzyżowych. Możliwość wystąpienia reakcji krzyżowej tłumaczy się podobną budową molekuł alergenowych.
Testy oparte na ekstraktach alergenowych nie umożliwiają rozróżnienia uczulenia pierwotnego od wyniku dodatniego spowodowanego reakcją krzyżową, podczas gdy diagnostyka molekularna alergii ma taki potencjał [22].
Zatem oznaczenie sIgE wobec molekuł alergenowych u pacjentów z uczuleniem wieloważnym może ułatwić rozróżnienie pierwotnego uczulenia od wyniku dodatniego spowodowanego wystąpieniem reakcji krzyżowych [23]. Wykonanie testu z użyciem molekuł u pacjenta z uczuleniem wieloważnym może wiązać się ze złagodzeniem zaleceń odnośnie unikania ekspozycji na pewne alergeny [22].
Diagnostyka molekularna a ryzyko anafilaksji
Dzięki poznaniu ryzyka wystąpienia reakcji ogólnoustrojowej uczulenia na poszczególne molekuły w obrębie danych rodzin molekuł (Rycina nr 1), określenie profilu uczulenia z użyciem narzędzi diagnostyki molekularnej może ułatwić odpowiedź na pytanie czy istnieje u pacjenta ryzyko wystąpienia ciężkiej reakcji ogólnoustrojowej. Wykonanie testów opartych na ekstraktach alergenowych może nie dostarczać wystarczającej informacji na temat ryzyka wystąpienia groźnych objawów anafilaktycznych, np.: uczulenie na niektóre molekuły alergenów pokarmowych jak, np. Ara h 1, Ara h 2, Ara h 3 oraz Ara h 9 orzecha ziemnego, wiąże się z dużym prawdopodobieństwem wystąpienia wstrząsu anafilaktycznego. Podczas gdy, uczulenie na Ara h 8 rzadko jest przyczyną reakcji uogólnionej, może być natomiast związane z reakcjami krzyżowymi z pewnymi alergenami wziewnymi, np. brzozą (Bet v 1), olchą (Aln g 1) czy leszczyną (Cor a 1) [23]. U pacjentów uczulonych na orzechy włoskie ryzyko wystąpienia ogólnoustrojowych reakcji jest większe, gdy w ich surowicy występują sIgE wobec molekuł Jug r 1 i Jug r 3 .
Dokładne opracowanie profilu uczulenia pacjenta na podstawie wyników testów molekularnych może przyczynić się do zrezygnowania z prób prowokacyjnych, które także wiążą się z ryzykiem wystąpienia ogólnoustrojowych reakcji.
Ponadto, uczulenie na kilka molekuł pochodzących z danego źródła alergenowego może pozwolić na przewidywanie nasilenia objawów. Wykazano albowiem, że otrzymywane wyniki dodatnie wobec wielu molekuł pochodzących z jednej rodziny wiążą się z większym nasileniem objawów [24]. Potwierdzenie uczulenia jedynie wobec danego ekstraktu alergenowego nie niesie informacji na temat prawdopodobieństwa wystąpienia ciężkiej reakcji ogólnoustrojowej [23].
Dlatego też u pacjentów z uczuleniem wobec alergenów pokarmowych, zwłaszcza z epizodem wstrząsu w przeszłości, zdiagnozowanych na podstawie testów wykorzystujących tylko ekstrakty alergenowe, warto poszerzyć diagnostykę o testy do diagnostyki molekularnej alergii IgE-zależnej.
Diagnostyka molekularna a strategia terapeutyczna
Lekarz diagnozujący alergię przy pomocy multiparametrowych testów do diagnostyki molekularnej, otrzymuje informacje na temat pacjenta, na podstawie których może dostosować zalecenia terapeutyczne do jego indywidualnego profilu uczulenia.
Wyniki testów molekularnych pozwalają ustalić czy pacjent musi kategorycznie unikać kontaktu z konkretnym źródłem alergenowym ze względu na wysokie ryzyko ciężkiej ogólnoustrojowej reakcji, czy też ekspozycja na dany alergen będzie wiązała się z wystąpieniem u pacjenta objawów łagodnych, np. nieżytu nosa [25]. Wiedza ta pozwala personalizować zalecenia terapeutyczne i przekłada się na jakość życia pacjenta (brak konieczności rygorystycznego unikania pewnych pokarmów, świadomość braku ryzyka ciężkich reakcji) [19].
LIPOKALINY:
- Can f 1 i Can f 2 pies, Fel d 4 kot, Equ c 1 koń oraz Bos d 2 i Bos d 5 krowa
Znajdują się w ślinie, moczu, surowicy i naskórku zwierząt sierściowych
Główną drogą narażenia na te alergeny są drogi oddechowe, za wyjątkiem alergenu Bod d 5 (P-laktoglobulina) głównego alergenu mleka krowiego
Zazwyczaj niski stopień reaktywności krzyżowej
TROPOMIOZYNY:
- Ani s 3 nicienie (pasożyty z rodziny Anisakidae), Der p 10 roztocze kurzu domowego, Hel as 1 ślimak, Lit v 1 krewetka, Per a 7 karaluch, Uro du 1 kalmar, Ven ga 1 małż
Występują w skorupiakach, roztoczach, karaluchach i nicieniach
Alergizują nawet po obróbce termicznej, odporne na enzymy trawienne
Alergeny pokarmowe często wywołują silne reakcje ogólnoustrojowe, zespół OAS
PARWALBUMINY:
- Mer mr 1 morszczuk, Cyp c 1 karp, Gad c 1 dorsz, Onc m 1 pstrąg, Sal s 1 łosoś, Thu a 1 tuńczyk
Najwyższe ich stężenie znajduje się w mięśniach ryb
Odporne na działanie temperatury i enzymy trawienne
Narażenie na te alergeny występuje zazwyczaj drogą pokarmową, ale reakcje mogą również nastąpić poprzez wdychanie oparów podczas smażenia ryb
Wysoki stopień reaktywności krzyżowej pomiędzy białkami pochodzącymi od różnych gatunków ryb; możliwe jednak również reakcje na wybrane pojedyncze molekuły z rodziny parwalbumin
ALBUMINY SUROWICZE:
- Bos d 6 krowa (mięso, mleko), Can f 3 pies, Fel d 2 kot, Equ c 3 koń, Gal d 5 jajo kurze
Występują w ślinie, moczu, naskórku, surowicy i mięsie zwierząt
Narażenie na te alergeny zazwyczaj występuje poprzez drogi oddechowe, ale również poprzez drogę pokarmową w przypadku spożycia mięsa zwierząt czy jaja kurzego
Są białkami wrażliwymi na działanie temperatury
Wysoki stopień reaktywności krzyżowej pomiędzy białkami pochodzącymi od różnych gatunków zwierząt
Kolejną zaletą diagnostyki molekularnej jest większa czułość diagnostyczna w porównaniu do ekstraktów alergenowych. Dla przykładu, udowodnione znaczenie kliniczne i możliwość oznaczania sIgE wobec molekuł brzoskwini było jedynie wobec Pru p 1, Pru p 3, Pru p 4. W swoim badaniu Vitte i in., pokazali grupę pacjentów, którzy mieli reakcje anafilaktyczną indukowaną spożyciem brzoskwini, mając negatywne wyniki sIgE wobec brzoskwini i jej ww. molekuł, a dodatnie wyniki testów skórnych i BAT. Niemal wszyscy z nich mieli dodatni wynik wobec niedawno opisanej i możliwej również od niedawna do testowania molekuły Pru p 7 [26]. Odkrycie tej molekuły i możliwość jej oznaczania zrewolucjonizować może podejście do uczulenia wobec brzoskwini. Badania wykazały, że molekuła ta jest jeszcze bardziej odporna na trawienie i obróbkę termiczną niż Pru p 3 (rodzina nsLTP) [27]. Istnieją doniesienia, że obecność w surowicy immunoglobulin E specyficznych wobec Pru p 7 może wiązać się z wystąpieniem objawów ogólnoustrojowych [26, 28].
| Uczulenie na pojedyncze lub kilka alergenów wziewnych | |
|---|---|
| Klasyfikacja do immunoterapii | Mnogie uczulenie na pytki |
| Alergia na owady błonkoskrzydłe | |
| Anafilaksja po pokarmach, przy współudziale kofaktorów | |
| Anafilaksja | Opóźniona anafilaksja po mięsie czerwonym |
| Anafilaksja idiopatyczna | |
| Alergia na latex | |
| Polisensytyzacja | Wspótwystępowanie uczulenia na alergeny wziewne i pokarmowe |
| Alergia pokarmowa | Ocena ryzyka ciężkości reakcji alergicznych |
| Identyfikacja niespodziewanych źródeł uczulenia |
Powyższy przykład dobrze obrazuje także inną zaletę diagnostyki molekularnej przy użyciu najnowszych testów, albowiem testy III generacji mogą być stale aktualizowane w oparciu o najnowsze odkrycia, tak by badały uczulenie wobec nowo-odkrytych molekuł istotnych klinicznie [22].
Czynnikami sprzyjającymi poznaniu nowych molekuł alergenowych jest ich wysoka koncentracja w źródle czy też podobieństwo do już odkrytych molekuł [29]. Jednak to, że dana molekuła alergenowa nie została jeszcze zidentyfikowana, nie oznacza, że nie może być ona silnym alergenem [22]. Tak właśnie było w przypadku molekuły Der p 23 (trzeci główny alergen Dermatophagoides pteronyssinus – roztocze kurzu domowego), która dzięki zaawansowanym technikom identyfikacji została opisana i uznana za klinicznie istotną jak Der p 1 i Der p 2 [30]. Posiadając obecnie wiedzę na temat Der p 23, można zweryfikować pacjentów z objawami sugerującymi alergię na roztocze a mającymi ujemne wyniki testów serologicznych. Można również zweryfikować pod kątem występowania sIgE wobec Der p 23 pacjentów bez powodzenia prowadzonej immunoterapii roztoczami kurzu domowego. Warto również podkreślić fakt, iż w większości przypadków ekstrakty w szczepionkach stosowanych do odczulania standaryzowane są jedynie pod kątem zawartości w nich Der p 1 i Der p 2 [13]. Dynamiczny rozwój diagnostyki molekularnej alergii pozwala na stałe rozszerzanie dostępnych do testowania molekuł alergenowych [22].
Immunoglobuliny E specyficzne wobec konkretnych molekuł alergenowych mogą być obecne w surowicy pacjentów na długo przed pojawieniem się klinicznych objawów alergii, a monitorowanie ich występowania w surowicy krwi pozwala na prognozowanie klinicznego obrazu alergii.
Wykazano, że uczulenie na pyłek trawy często rozpoczyna się jako uczulenie monowalentne. Z czasem w surowicy pojawiają się kolejne sIgE wobec następnych molekuł, często w określonej kolejności. W przypadku uczulenia na pyłek tymotki łąkowej, na początku obecne są sIgE wobec Phl p 1. Po miesiącach lub latach w surowicy pojawiają się przeciwciała E swoiste wobec Phl p 4, Phl p 5, Phl p 2, Phl p 6 i Phl p 11. Dopiero po pojawieniu się objawów alergii na pyłek tymotki w surowicy są wykrywalne sIgE wobec Phl p 12 czy Phl p 7. Badania Hatzlera i in. pokazało, że u około 2/3 dzieci, u których w wieku 3 lat rozpoznano uczulenie na pyłek tymotki – w wieku 12 lat miało alergiczny nieżyt nosa w sezonie pylenia tymotki [31]. Podobne obserwacje są udokumentowane w przypadku uczulenia wobec brzozy [32].
Możemy zatem stwierdzić na tej podstawie, że testy oparte na molekułach alergenowych można wykorzystać do monitorowania zmian profilu uczulenia konkretnego pacjenta, obserwowania zależności pomiędzy uczuleniem a objawami klinicznymi oraz dostosowania zaleceń terapeutycznych [33].
Testy molekularne a immunoterapia
Ogromną zaletą testów molekularnych jest możliwość na ich podstawie kwalifikacji do immunoterapii, co podnosi zarówno jej skuteczność i efektywność. Celem swoistej immunoterapii (SIT) jest zmodyfikowanie odpowiedzi układu immunologicznego wobec konkretnego alergenu podawanego podskórnie lub podjęzykowo [2]. Odpowiedni dobór preparatu alergenowego ma kluczowe znaczenie dla powodzenia immunoterapii. O ile w przypadku pacjentów z alergią monowalentną identyfikacja istotnego klinicznie alergenu i określenie składu preparatu alergenowego do SIT nie stanowi problemu, o tyle u pacjentów z alergią wieloważną zidentyfikowane alergenu odpowiedzialnego za występowanie alergii może nastręczać już kłopotów [25, 34]. Dlatego też, szczególnie w grupie chorych kwalifikowanych do immunoterapii, precyzyjne określenie alergenu odpowiedzialnego za objawy jest niezbędne dla sukcesu terapeutycznego. Warto mieć na uwadze, że w pewnych przypadkach wywiad w oparciu o objawy kliniczne oraz wyniki SPT nie wystarczają do wyjaśnienia przyczyny uczulenia [35]. U pacjentów z uczuleniem wieloważnym wykonanie testów opartych na molekułach alergenowych może ułatwić dobór odpowiednich składników stosowanych w SIT. Przykładowo, pacjent może mieć w surowicy sIgE wobec molekuł trawy Phl p 1 oraz Phl p 5 (potwierdzone uczulenie na pyłek tymotki łąkowej), ale nie stwierdza się u niego obecności sIgE wobec molekuły brzozy Bet v 1 (brak uczulenia na brzozę). Jeśli dodatkowo w surowicy tego pacjenta obecne są również sIgE wobec Phl p 12 (profilina), to można podejrzewać, że dodatni wynik SPT wobec antyge nu brzozy (także zawierającego profilinę), był spowodowany reakcją krzyżową. Tak więc u tego pacjenta należy zastosować SIT wobec pyłku tymotki łąkowej, ale nie wobec brzozy. W takich przypadkach diagnostyka molekularna pozwala dobrać odpowiedni preparat do SIT.
Badania Sastre i in. pokazują, że wykonanie testów molekularnych i poznanie molekuł odpowiedzialnych za reakcje alergiczne u pacjentów może prowadzić do konieczności zmiany SIT nawet u ponad 50% pacjentów, u których wdrożono immunoterapię na podstawie jedynie wyników SPT [36].
Testy do diagnostyki molekularnej
Obecnie najbardziej kompleksowymi narzędziami do diagnostyki molekularnej alergii są testy III generacji, jak test ALEX® czy platforma diagnostyczna FABER®. Test ALEX® pozwala oznaczyć sIgE wobec 156 ekstraktów oraz 126 molekuł alergenowych jednocześnie. Oznacza to, że z jednej próbki badanej (surowicy krwi pacjenta) możemy określić czy dany pacjent jest uczulony wobec jednego czy wielu źródeł alergenowych, na jaką molekułę lub molekuły, z jakich rodzin białek, czy uczulenie pacjenta ma charakter pierwotny czy wtórny (jako skutek reakcji krzyżowej).
Platforma diagnostyczna FABER®
Platforma diagnostyczna FABER® składa się nie tylko z testu obejmującego podobna liczbę źródeł, ekstraktów i molekuł alergenowych, ale również dedykowanej do tego testu specjalnej platformy ułatwiającej interpretację wyniku testu zarówno lekarzowi prowadzącemu, jak i pacjentowi.
Podążając za modelem diagnostycznym „top – down”, dostępne testy III generacji umożliwiające badanie molekuł i ekstraktów alergenowych, zapewniają drugi i trzeci etap diagnostyki alergii w jednym kroku diagnostycznym. Wpływa to korzystnie na oszczędność czasu niezbędnego do postawienia diagnozy w całym procesie diagnostycznym. Warto zaznaczyć, że jednoczesne oznaczenie w surowicy pacjenta sIgE wobec niemal 300 alergenów, w tym ekstraktów i molekuł jest zgodne również z punktem widzenia zwolenników modelu „bottom – up” [3].
Rozwój diagnostyki molekularnej w chorobach alergicznych coraz bardziej przybliża nas do medycyny spersonalizowanej – czyli leczenia alergii ściśle dopasowanego do indywidualnego profilu uczulenia danego pacjenta uzyskanego za pomocą testów molekularnych. Obecność w surowicy sIgE wobec konkretnych molekuł może ułatwić określenie: Czy i w jakim stopniu pacjent ma ograniczyć kontakt z alergenem? Co więcej, pomaga także ustalić czy ma również unikać ekspozycji na inne alergeny, pomiędzy którymi mogą zachodzić reakcje krzyżowe. Zebrane korzyści z zastosowania diagnostyki molekularnej przedstawiono w tabeli nr 3.
| precyzyjnie określa alergen/y odpowiedzialne za objawy | |
|---|---|
| ułatwia rozróżnienie pierwotnego uczulenia od reakcji krzyżowych | |
| DIAGNOZA | zwiększa czułość diagnostyczną w porównaniu do testów bazujących na ekstraktach alergenowych |
| pozwala na monitorowanie zmian profilu uczulenia konkretnego pacjenta, obserwowanie zależności pomiędzy uczuleniem a objawami klinicznymi | |
| zmniejsza liczbę wizyt oraz skraca czas potrzebny do postawienia prawidłowej diagnozy | |
| OCENA RYZYKA | pozwala na prognozowanie klinicznego obrazu alergii |
| pozwala oszacować ryzyko wystąpienia u pacjenta ciężkich ogól- noustrojowych reakcji, co może przyczynić się do zrezygnowania z prób prowokacyjnych, które wiążą się z ryzykiem wstrząsu | |
| LECZENIE | pozwala personalizować zalecenia terapeutyczne do indywidualnego profilu uczulenia |
| skraca czas kwalifikacji do SIT oraz podnosi jej skuteczność i efektywność |
Rozbieżności w wynikach pomiędzy ekstraktem a jego molekułami alergenowymi
Poziomy stężeń sIgE wykonanych w oparciu o molekuły alergenowe nie zawsze muszą zgadzać się z wynikami testów wykorzystujących ekstrakty alergenowe. Może zaistnieć sytuacja, gdy w surowicy pacjenta zostaną wykryte przeciwciała E specyficzne wobec ekstraktu, ale nie zaobserwuje się sIgE wobec molekuł z tego źródła alergenowego, co dany ekstrakt. Powodem takiej rozbieżności może być uczulenie pacjenta na molekuły ekstraktu, które nie są jeszcze dostępne do badania. Możliwy jest także wynik, gdzie u pacjenta w surowicy nie wykryjemy sIgE wobec ekstraktu, a wykryjemy sIgE wobec molekuł z tego źródła alergenowego (Tabela nr 4). Powyższa sytuacja może być wytłumaczona niższą czułością diagnostyczną testu opartego o badanie sIgE wobec ekstraktu niż czułość diagnostyczna testu badającego sIgE wobec molekuł alergenowych, Ponadto, molekuły rozpoznane przez sIgE mogą nie występować w ekstrakcie lub ich liczba w ekstrakcie może być zbyt mała, by otrzymać dodatni wynik tak jak jest w przypadku ekstraktu soi i jej molekuły Gly m 4, ekstraktu alergenu psa i jego molekuły Can f 5 czy ekstraktu roztoczy Dermatophagoides pteronyssinus i ich molekuły Der p 23 [13, 37].
| Molekuła | Ekstrakt | Wyjaśnienie |
|---|---|---|
| + | - | brak lub mała zawartość tej molekuły w ekstrakcie. Badania w oparciu o ekstrakty mają niższą czułość |
| - | + | w surowicy krwi obecne są sIgE wobec molekuł badanego alergenu, które nie były badane w danym teście (np. ze względu na to, że nie są jeszcze dostępne. Do komercyjnego testowania). Wynik może być związany z obecnością przeciwciał anty-CCD w surowicy krwi |
| - | - | Z dużym prawdopodobieństwem wyklucza IgE zależne podłoże objawów alergii |
Ograniczenia metody
Decydując się na oznaczenie w surowicy pacjenta sIgE wobec molekuł alergenowych, należy mieć na uwadze, że tak samo jak w przypadku oznaczeń sIgE wobec ekstraktów alergenowych, potwierdzenie ich obecności nie świadczy o chorobie alergicznej, a jest dowodem uczulenia [21].
Potwierdzenie obecności sIgE w surowicy pacjenta ma znaczenie kliniczne wyłącznie w obliczu współistnienia objawów alergii [13].
Biorąc po uwagę powyższe informacje, należy pamiętać, że zarówno wyniki sIgE wobec ekstraktów alergenowych, jak i molekuł muszą być zawsze interpretowane w oparciu o wywiad kliniczny i objawy danego pacjenta [13].
Warto zauważyć, że przeciwciała E swoiste wobec danego alergenu mogą być obecne w surowicy pacjentów na długo przed pojawieniem się objawów alergii a ich obecność w surowicy jest uznawana za czynnik ryzyka rozwoju choroby alergicznej [22, 38].
Choć narzędzia diagnostyki molekularnej są kompleksowe i zawierają wiele istotnych klinicznie alergenów, należy pamiętać, że na ten moment nie opisano wszystkich molekuł alergenowych w wielu źródłach alergenowych. Dlatego też, wynik ujemny w odniesieniu do poszczególnych molekuł, należy zawsze interpretować w odniesieniu do ekstraktów, ponieważ nie możemy mieć pewności, że danego pacjenta uczula molekuła, która nie była badana danym testem [22]. Zaletą testów III generacji, jak system diagnostyczny FABER® czy test ALEX® jest jednoczesne badanie ekstraktów alergenowych i ich istotnych klinicznie molekuł. Uzyskanie wyniku negatywnego przy użyciu testów multiparametrowych w diagnozowaniu alergii zasadniczo wyklucza alergię w mechanizmie IgE-zależnym [13].
Oprócz tych testów pozwalających na tak obszerną diagnostykę, są testy panelowe pozwalające na diagnostykę molekularną celowaną, np. Polycheck® Rekombinanty Pyłki, zawierający ekstrakt brzozy oraz jej dwie główne molekuły Bet v 1 i Bet v 2 oraz ekstrakt tymotki łąkowej i jej główne molekuły Phl p 1 i Phl p 5 oraz molekuły Phl p 7 i Phl p 12, czy panel Polycheck® Rekombinanty Roztocze zawierający ekstrakty Dermatophagoides farinae oraz Dermatophagoides pteronyssinus oraz jego istotne klinicznie molekuły, jak: Der p 1, Der p 2, Der p 10 i Der p 23. Obydwa w.w. panele multiparametrowe są pomocne do klasyfikacji pacjentów do immunoterapii, będą jednocześnie alternatywą pomiędzy pojedynczymi oznaczeniami sIgE a multiparametrowymi testami jak ALEX® i FABER®.
Podsumowanie
Obecnie multiparametrowe testy oparte o molekuły alergenowe i ekstrakty alergenowe umożliwiają określenie indywidualnego profilu uczulenia danego pacjenta. Pozwalają one zróżnicować objawy alergii pierwotnej od objawów alergicznych spowodowanych występowaniem reakcji krzyżowych. Ponadto, cechują się większą czułością i swoistością diagnostyczną niż testy wykorzystujące jedynie ekstrakty. Warto podkreślić, że dzięki użyciu diagnostyki molekularnej można ocenić ryzyko wystąpienia u pacjenta ciężkich reakcji ogólnoustrojowych. Testy te pomocne są również w zakresie ustalania zaleceń terapeutycznych – ograniczania kontaktu z wybranym alergenem czy kwalifikacji do immunoterapii. Diagnostyka molekularna alergii pozwala na spersonalizowanie zaleceń terapeutycznych, tak aby mogłyby być one dopasowane do potrzeb konkretnych pacjentów, co znacząco może przełożyć się na poprawę jakości życia chorych z alergią.
Prof. dr hab. n. med. Bolesław Samoliński
Dr n. med. Emilia Majsiak
Reprint artykuł, który ukazał się w czasopiśmie Alergia do pobrania tutaj
Piśmiennictwo: 1. Samoliński B., et al. Epidemiologia chorób alergicznych w Polsce (ECAP). Alergologia Polska, 2014. 1(1): p. 10-18. 2. Canonica G. W., et al. A WAO – ARIA – GA(2)LEN consensus document on molecular-based allergy diagnostics. World Allergy Organ J, 2013. 6(1): p. 17. 3. Heffler E., et al. Extended IgE profile based on an allergen macroarray: a novel tool for precision medicine in allergy diagnosis. World Allergy Organ J, 2018. 11(1): p. 7. 4. Matricardi PM., et al. EAACI Molecular Allergology User’s Guide. Pediatr Allergy Immunol, 2016: p. 1-250. 5. Zgorzelska-Kowalik J., et al. Cross-reactive carbohydrate determinants in diagnostics of occupational allergy. Medycyna Pracy, 2010. 61(1): p. 79-89. 6. Wiszniewska M., et al. Identification of cross-reactive carbohydrate determinants in subjects reporting work-related respiratory symptoms. Int J Occup Med Environ Health, 2015. 28(1): p. 90-101. 7. Altmann F. Coping with cross-reactive carbohydrate determinants in allergy diagnosis. Allergo J Int, 2016. 25(4): p. 98-105. 8. Malandain H. IgE-reactive carbohydrate epitopes–classification, cross-reactivity, and clinical impact. Eur Ann Allergy Clin Immunol, 2005. 37(4): p. 122-8. 9. Mari A., et al. Evaluation by double-blind placebo-controlled oral challenge of the clinical relevance of IgE antibodies against plant glycans. Allergy, 2008. 63(7): p. 891-6. 10. Mari A. IgE to cross-reactive carbohydrate determinants: analysis of the distribution and appraisal of the in vivo and in vitro reactivity. Int Arch Allergy Immunol, 2002. 129(4): p. 286-95. 11. Majsiak E. and Buczyłko K. Krzyżowo reagujące determinanty węglowodanowe (CCD) i bloker CCD w diagnostyce alergii. Alergia, 2017. 4: p. 39-42. 12. Csonka P. Molecular allergology. User’s Guide for Allergen Components IgE Tests. Hämeen Kirjapaino Oy, 2018. 13. Kleine-Tebbe J. and Jakob T. Molecular Allergy Diagnostics. 2017: Springer. 14. Kowalski M. L., et al. Risk and safety requirements for diagnostic and therapeutic procedures in allergology: World Allergy Organization Statement. World Allergy Organ J, 2016. 9(1): p. 33. 15. Canonica GW., Ansotegui IJ., and Pawankar R. Diagnostyka Molekularna Alergii (MA). Przewodnik kieszonkowy. NA PODSTAWIE DOKUMENTU KONSENSUSU WAO-ARIA-GA2LEN 2013. World Allergy Organization Journal, 2013. 6. 16. Majsiak E. Faber. Nowa generacja testów molekularnych do diagnozowania alergii IgE-zależnych. Alergia, 2017. 1. 17. Jensen-Jarolim E., Jensen A. N., and Canonica G. W. Debates in allergy medicine: Molecular allergy diagnosis with ISAC will replace screenings by skin prick test in the future. World Allergy Organ J, 2017. 10(1): p. 33. 18. Luengo O. and Cardona V. Component resolved diagnosis: when should it be used? Clin Transl Allergy, 2014. 4: p. 28. 19. Mothes-Luksch N., et al. Allergy diagnosis from symptoms to molecules, or from molecules to symptoms: a comparative clinical study. World Allergy Organ J, 2018. 11(1): p. 22. 20. Migueres M., et al. Types of sensitization to aeroallergens: definitions, prevalences and impact on the diagnosis and treatment of allergic respiratory disease. Clinical and Translational Allergy, 2014. 4(1): p. 1-8. 21. Haftenberger M., et al. Prevalence of sensitisation to aeraoallergens and food allergens: results of the German Health Interview and Examination Survey for Adults (DEGS1). Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz, 2013. 56(5- 6): p. 687-697. 22. Alessandri C., et al. Diagnosing allergic sensitizations in the third millennium: why clinicians should know allergen molecule structures. Clin Transl Allergy, 2017. 7: p. 21. 23. Jakob T., et al. Molecular allergy diagnostics using multiplex assays: methodological and practical considerations for use in research and clinical routine: Part 21 of the Series Molecular Allergology. Allergo J Int, 2015. 24: p. 320-332. 24. Nicolaou N. and Custovic A. Molecular diagnosis of peanut and legume allergy. Curr Opin Allergy Clin Immunol, 2011. 11(3): p. 222-8. 25. Rogala B. Immunoterapia alergenowa w uczuleniu wieloważnym Alergologia Polska – Polish Journal of Allergology 2018. 5(3): p. 133-136. 26. Vitte J., et al. Multiplex method for IgE determination: a report of six severe peach allergic patients from Southern France. European Academy of Allergy and Clinical Immunologym, 17 – 21 June 2017, Helsinki, Finland – poster 1206, 2017. 27. Tuppo L., et al. Structure, stability, and IgE binding of the peach allergen Peamaclein (Pru p 7). Biopolymers, 2014. 102(5): p. 416-25. 28. Inomata N., et al. Identification of peamaclein as a marker allergen related to systemic reactions in peach allergy. Ann Allergy Asthma Immunol, 2014. 112(2): p. 175-177 e3. 29. Mari A., et al. Proteomic analysis in the identification of allergenic molecules. Expert Rev Proteomics, 2010. 7(5): p. 723-34. 30. Weghofer M., et al. Identification of Der p 23, a peritrophin-like protein, as a new major Dermatophagoides pteronyssinus allergen associated with the peritrophic matrix of mite fecal pellets. J Immunol, 2013. 190(7): p. 3059-67. 31. Hatzler L., et al. Molecular spreading and predictive value of preclinical IgE response to Phleum pratense in children with hay fever. J Allergy Clin Immunol, 2012. 130(4): p. 894-901 e5. 32. Westman M., et al. Early childhood IgE reactivity to pathogenesis-related class 10 proteins predicts allergic rhinitis in adolescence. J Allergy Clin Immunol, 2015. 135(5): p. 1199-206 e1-11. 33. Lucas J. M. Microarrays: Molecular allergology and nanotechnology for personalised medicine (II). Allergol Immunopathol (Madr), 2010. 38(4): p. 217-23. 34. Calderon M. A., et al. Multiple-allergen and single-allergen immunotherapy strategies in polysensitized patients: looking at the published evidence. J Allergy Clin Immunol, 2012. 129(4): p. 929-34. 35. Ciprandi G., et al. Characteristics of patients with allergic polysensitization: the POLISMAIL study. Eur Ann Allergy Clin Immunol, 2008. 40(3): p. 77-83. 36. Sastre J., et al. How molecular diagnosis can change allergen-specific immunotherapy prescription in a complex pollen area. Allergy, 2012. 67(5): p. 709-11. 37. Gaweł J., et al. Częstość występowania wybranych epitopów reakcji alergenowych u dzieci z objawami alergii. Alergia Astma Immunologia, 2013. 18(4): p. 241-250. 38. Cox L. Overview of serological-specific IgE antibody testing in children. Curr Allergy Asthma Rep, 2011. 11(6): p. 447-453.
