
Zakażenie Clostridioides difficile – objawy, przyczyny, badania, leczenie
- Jak dochodzi do zakażenia Clostridioides difficile?
- Clostridioides difficile – objawy zakażenia
- Postacie CDI
- Podział ze względu na miejsce zakażenia
- Skala problemu
- Clostidioides difficile – badania i diagnostyka
- Clostidioides difficile – leczenie i nowoczesne terapie
- Clostidioides difficile – leczenie w domu i zasady postępowania
- Clostidioides difficile – powikłania zakażenia
- Znaczenie profilaktyki
Zakażenie Clostridioides difficile (CDI, Clostridioides difficile infection) należy obecnie do najczęstszych zakażeń związanych z opieką zdrowotną. Chorobę wywołuje beztlenowa bakteria Gram-dodatnia Clostridioides difficile (dawniej Clostridium difficile), która naturalnie występuje w środowisku oraz w przewodzie pokarmowym człowieka.

Jak dochodzi do zakażenia Clostridioides difficile?
Do zakażenia dochodzi najczęściej drogą fekalno-oralną. Przetrwalniki bakterii mogą zostać przeniesione z zanieczyszczonych powierzchni, sprzętu medycznego lub rąk personelu medycznego do przewodu pokarmowego człowieka.
Kluczową rolę w rozwoju choroby odgrywa zaburzenie naturalnej mikrobioty jelitowej. W prawidłowych warunkach bakterie jelitowe chronią organizm przed nadmiernym namnażaniem patogenów. Gdy równowaga mikrobiomu zostaje zachwiana, najczęściej po zastosowaniu antybiotyków, C. difficile może zacząć intensywnie namnażać się w jelicie grubym i produkować toksyny uszkadzające nabłonek jelitowy.
Szczególnie problematyczna jest zdolność bakterii do tworzenia przetrwalników, które mogą przez długi czas utrzymywać się w środowisku szpitalnym i pozostają odporne na wiele standardowych środków dezynfekcyjnych.
Najważniejsze czynniki ryzyka
Antybiotykoterapia
Najważniejszym czynnikiem ryzyka zakażenia pozostaje antybiotykoterapia. Ryzyko zakażenia jest największe bezpośrednio po zakończeniu leczenia i może utrzymywać się jeszcze przez kilka tygodni. Największe znaczenie przypisuje się stosowaniu:
- fluorochinolonów,
- klindamycyny,
- cefalosporyn,
- karbapenemów
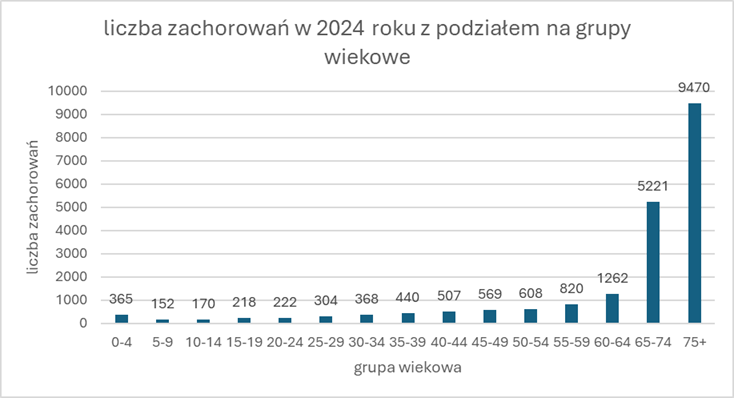
Wiek
Ryzyko zachorowania wyraźnie wzrasta wraz z wiekiem. Największą zapadalność obserwuje się u osób po 65. roku życia. Pacjenci w podeszłym wieku są również bardziej narażeni na ciężki przebieg choroby oraz rozwój powikłań.
Hospitalizacja
Szpitale i domy opieki należą do miejsc szczególnie sprzyjających transmisji bakterii. Długotrwały pobyt w placówkach medycznych zwiększa ryzyko kontaktu z przetrwalnikami C. difficile.
Choroby przewlekłe
Wyższe ryzyko zakażenia dotyczy również osób z chorobami osłabiającymi odporność organizmu, między innymi:
- niewydolnością nerek,
- niewydolnością wątroby,
- chorobami nowotworowymi,
- HIV,
- przewlekłymi zapalnymi chorobami jelit.
U osób starszych oraz pacjentów z zaburzoną mikrobiotą jelitową śmiertelność związana z ciężkimi postaciami CDI może sięgać nawet 25%.
Clostridioides difficile – objawy zakażenia
Najczęstszym objawem zakażenia Clostridioides difficile jest wodnista biegunka. Choroba odpowiada za około 15–25% przypadków biegunki poantybiotykowej oraz za większość przypadków rzekomobłoniastego zapalenia jelita grubego.
Do typowych objawów należą:
- wodnista biegunka,
- bóle brzucha,
- gorączka,
- nudności,
- wymioty,
- utrata apetytu,
- osłabienie.
W cięższych przypadkach może dochodzić do znacznego odwodnienia, zaburzeń elektrolitowych oraz objawów ogólnoustrojowych.
Postacie CDI
Nawracające zakażenie CDI
Nawrót rozpoznaje się wtedy, gdy kolejny epizod choroby pojawia się od 2 do 8 tygodni po ustąpieniu wcześniejszych objawów. Nawroty należą do największych problemów terapeutycznych i znacząco zwiększają ryzyko kolejnych powikłań.
Ciężka postać CDI
Ciężkie zakażenie przebiega z nasilonym stanem zapalnym jelita grubego oraz objawami ogólnoustrojowymi wywołanymi toksynami bakteryjnymi. Pacjenci często wymagają hospitalizacji, a niekiedy również leczenia chirurgicznego.
Piorunująca postać CDI
Najgroźniejszą formą zakażenia jest postać piorunująca, przebiegająca z hipotensją, wstrząsem, niedrożnością jelit lub toksycznym rozdęciem okrężnicy. Jest to stan bezpośredniego zagrożenia życia.
Podział ze względu na miejsce zakażenia
Z epidemiologicznego punktu widzenia wyróżnia się zakażenia:
- związane z opieką zdrowotną,
- pozaszpitalne,
- o nieustalonym pochodzeniu.
Ognisko epidemiczne CDI
O ognisku epidemicznym mówi się wtedy, gdy w określonym czasie i miejscu wystąpią co najmniej dwa powiązane ze sobą przypadki zakażenia, a liczba zachorowań przekracza poziom typowo obserwowany w danej placówce.
Skala problemu
Clostridioides difficile pozostaje jedną z najczęstszych przyczyn zakażeń związanych z opieką zdrowotną w Europie i w Polsce. Największy wzrost liczby przypadków obserwuje się w krajach wysoko rozwiniętych, gdzie częste stosowanie antybiotyków oraz starzenie się społeczeństw zwiększają ryzyko zachorowania.
Według danych epidemiologicznych częstość zakażeń C. difficile w Polsce w latach 2021–2024 utrzymywała się na poziomie około 55 przypadków na 100 tysięcy mieszkańców. W 2024 roku wskaźnik wyniósł 55,10/100 tys. mieszkańców, co wskazuje na utrzymujące się wysokie obciążenie systemu ochrony zdrowia.
Europejskie Centrum ds. Zapobiegania i Kontroli Chorób (ECDC) szacuje, że w krajach Unii Europejskiej każdego roku dochodzi do około 124 tysięcy szpitalnych zakażeń Clostridioides difficile. Bakteria należy obecnie do najczęściej wykrywanych patogenów odpowiedzialnych za zakażenia szpitalne w Europie.
Niepokój specjalistów budzi również narastająca lekooporność bakterii oraz dominacja hiperepidemicznego szczepu RT027, który odpowiada za cięższy przebieg choroby i częstsze nawroty zakażenia.
Szacuje się, że bezobjawowe nosicielstwo C. difficile występuje u około 3% zdrowych dorosłych. Wśród pacjentów hospitalizowanych odsetek ten może wzrastać nawet do 20–40%. Szczególnie wysoki poziom nosicielstwa obserwuje się u noworodków i niemowląt, u których może on sięgać nawet 50–60%, stopniowo zmniejszając się po pierwszym roku życia.
Clostidioides difficile – badania i diagnostyka
Rozpoznanie zakażenia opiera się przede wszystkim na objawach klinicznych oraz wynikach badań laboratoryjnych. Kluczowe znaczenie ma wykrycie toksyn produkowanych przez bakterię, ponieważ samo stwierdzenie obecności C. difficile w przewodzie pokarmowym nie oznacza jeszcze aktywnego zakażenia.
Bakteria produkuje trzy główne toksyny:
- enterotoksynę A,
- cytotoksynę B,
- toksynę binarną.
Toksyna A odpowiada głównie za rozwój stanu zapalnego jelita, natomiast toksyna B powoduje silne uszkodzenie komórek nabłonka i uznawana jest za główny czynnik ciężkiego przebiegu choroby. Niektóre szczepy wytwarzają również toksynę binarną, która dodatkowo zwiększa zjadliwość bakterii.
Testy laboratoryjne
Europejskie Towarzystwo Mikrobiologii Klinicznej i Chorób Zakaźnych zaleca wykonanie:
- testu wykrywającego obecność bakterii lub jej antygenów
- testu wykrywającego toksyny A i B.
Zasadność wykonania testów przedstawionych poniżej należy przedyskutować z lekarzem.
Sprawdź badania:
- Clostridioides difficile, antygen GDH i toksyna A/B w kale
- Clostridioides difficile oznaczenie genu GDH, toksyny A, toksyny B oraz binarnej (met. NAAT)
- Clostridioides difficile-toksyna B,toksyna binarna,obecność szczepu hiperepidemicznego (DNA) met. Real Time-PCR
Badania dodatkowe
W wybranych przypadkach wykonuje się:
- kolonoskopię,
- badania obrazowe jamy brzusznej,
- badania krwi oceniające stan zapalny i odwodnienie
Clostidioides difficile – leczenie i nowoczesne terapie
Leczenie farmakologiczne
Podstawą terapii pozostają antybiotyki celowane działające przeciwko Clostridioides difficile. Dobór leczenia zależy od ciężkości przebiegu choroby, wieku pacjenta oraz ryzyka nawrotów. W części przypadków konieczne jest także odstawienie antybiotyku, który doprowadził do zaburzenia mikrobioty jelitowej.
Nowoczesne metody leczenia
Coraz większe znaczenie mają nowoczesne terapie ukierunkowane na odbudowę mikrobiomu jelitowego oraz ograniczanie nawrotów choroby. Należą do nich:
- przeszczep mikrobioty jelitowej,
- immunoterapia,
- przeciwciała monoklonalne, np. bezlotoksumab.
Nowoczesne metody leczenia są szczególnie istotne u pacjentów z nawracającymi zakażeniami CDI.
Clostidioides difficile – leczenie w domu i zasady postępowania
Leczenie domowe możliwe jest wyłącznie przy łagodnym przebiegu choroby i zawsze powinno odbywać się pod kontrolą lekarza.
Nawadnianie
Biegunka prowadzi do utraty wody i elektrolitów, dlatego konieczne jest:
- picie dużej ilości płynów,
- stosowanie elektrolitów,
- lekkostrawna dieta.
Higiena
Aby ograniczyć ryzyko zakażenia innych domowników, należy:
- dokładnie myć ręce wodą z mydłem,
- regularnie dezynfekować toalety,
- używać osobnych ręczników.
Obserwacja objawów
Pacjent powinien monitorować:
- liczbę wypróżnień,
- temperaturę ciała,
- objawy odwodnienia.
W przypadku pogorszenia stanu konieczny jest pilny kontakt z lekarzem.
Clostidioides difficile – powikłania zakażenia
Nieleczone zakażenie może prowadzić do bardzo poważnych konsekwencji zdrowotnych.
Najgroźniejsze powikłania obejmują:
- toksyczne rozdęcie okrężnicy,
- perforacja jelita,
- sepsa,
- niewydolność wielonarządowa,
- nawracające zakażenia,
- zgon.
Szczególnie niebezpieczne są nawroty choroby, które mogą pojawić się nawet po skutecznym leczeniu.
Znaczenie profilaktyki
Eksperci podkreślają, że najważniejszym elementem profilaktyki pozostaje odpowiedzialne stosowanie antybiotyków. Nadużywanie leków przeciwbakteryjnych sprzyja zaburzeniom mikrobioty jelitowej i zwiększa ryzyko rozwoju CDI. Aby zmniejszyć ryzyko zakażenia, należy:
- stosować antybiotyki wyłącznie zgodnie z zaleceniami lekarza,
- przestrzegać higieny rąk,
- ograniczać niepotrzebne hospitalizacje,
- regularnie dezynfekować powierzchnie w placówkach medycznych,
- stosować środki sporobójcze.
Rosnąca liczba zakażeń Clostridioides difficile pokazuje, że problem ten pozostaje jednym z najważniejszych wyzwań współczesnej medycyny szpitalnej. Kluczowe znaczenie mają szybka diagnostyka, odpowiednie leczenie oraz skuteczna profilaktyka ograniczająca rozprzestrzenianie się bakterii.
Mgr Karolina Górska
Bibliografia
Kochanowski R., Lonser P. „Clostridioides difficile: zarys historyczny, czynniki ryzyka, objawy kliniczne, diagnostyka i leczenie”, Hygeia Public Health 2025, 57(2): 51–58.
Hryniewicz W., Martirosian G., Ozorowski T. (red.)., Zakażenia Clostridioides (Clostridium) difficile: epidemiologia, diagnostyka, terapia, profilaktyka., Narodowy Program Ochrony Antybiotyków, Warszawa, 2018.
Narodowy Instytut Zdrowia Publicznego PZH – PIB, Główny Inspektorat Sanitarny. (2025), Choroby zakaźne i zatrucia w Polsce w 2024 roku., Warszawa: NIZP PZH – PIB.
Surawicz CM, Brandt LJ, Binion DG, Ananthakrishnan AN, Curry SR, Gilligan PH, McFarland LV, Mellow M, Zuckerbraun BS. Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections. Am J Gastroenterol. 2013;108(4):478–498. PMID: 23439232
5. European Centre for Disease Prevention and Control (ECDC). Clostridioides difficile infections. Stockholm: ECDC. Online, dostęp: 13.05.2026.





